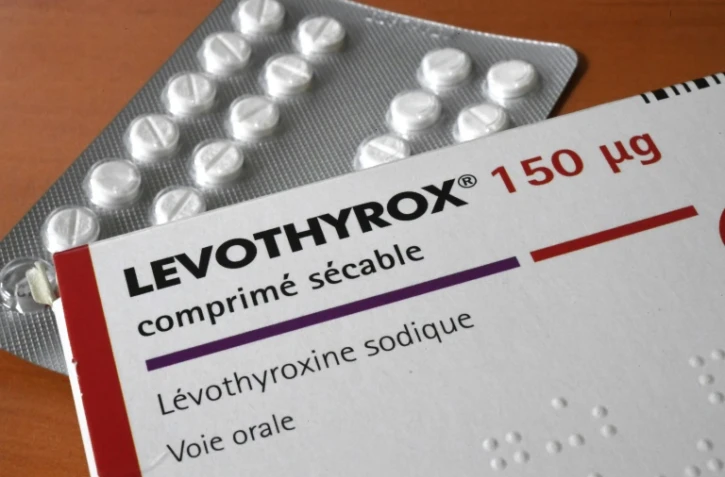
La justice s'est saisie vendredi du dossier Levothyrox et va enquêter après les plaintes de malades de la thyroïde victimes d'effets secondaires de la nouvelle formule de ce médicament, dont une ancienne version doit être de retour en pharmacie d'ici 15 jours.
L'enquête préliminaire a été confiée au pôle de santé publique du tribunal de grande instance de Marseille, dont la compétence s'étend jusqu'à Lyon, siège français du laboratoire allemand Merck qui produit ce médicament, a annoncé à l'AFP le procureur de la République de Marseille, Xavier Tarabeux. "Il faut que la vérité éclate, et que toutes les responsabilités pénales puissent être envisagées. Seule une enquête judiciaire le permettra", s'est félicité auprès de l'AFP Me David-Olivier Kaminski, qui a déjà déposé 12 plaintes au nom d'utilisatrices de Levothyrox, et en prépare "plusieurs dizaines" d'autres.
Il demande à la justice de se pencher sur la responsabilité de l'ancienne ministre socialiste de la Santé, Marisol Touraine, de l'Agence nationale de sécurité du médicament (ANSM), et du laboratoire. L'une de ses consoeurs, Me Marie-Odile Bertella-Geffroy, ex-juge du pôle santé publique de Paris et conseil de l'Association française des malades de la thyroïde, a déposé de son côté 51 plaintes.
Parmi les infractions visées par ces plaintes, la "mise en danger de la vie d'autrui" et la "tromperie" ou encore la "non-assistance à personne en danger".
Au total, trois millions de patients prennent ce médicament en France (premier marché mondial) pour soigner l'hypothyroïdie ou après une opération de cancer de la thyroïde. Selon le ministère de la Santé, plus de 9.000 personnes ont signalé des effets indésirables --crampes, maux de tête, vertiges, perte de cheveux-- attribués à la nouvelle formule du Levothyrox commercialisée depuis fin mars.
Une large partie des effets indésirables seraient liée à "des difficultés" à doser la nouvelle formule du Levothyrox, un médicament dont l'écart entre la dose efficace et la dose néfaste est faible, avait assuré lundi la ministre de la Santé Agnès Buzyn.
-"Premier pas"-
Vendredi, pour parer au plus urgent, elle a annoncé avoir "fait en sorte (...) que l'ancien Levothyrox soit accessible de façon à ce que ceux qui le réclament puissent le prendre", d'ici 15 jours. Un seul produit de substitution, appelé L-Thyroxine, existe pour le moment en France, mais des alternatives seront disponibles "dans un mois" et les patients pourront ainsi choisir ce "qui leur convient le mieux", a-t-elle ajouté.
Le retour à l'ancienne formule ne pourra se faire "que sur prescription médicale" et "ne pourra être proposée avec la même variété de dosage que l'actuelle formule", a précisé à l'AFP Thierry Hulot, patron des activités biopharmaceutiques de Merck Serono en France. La ministre a aussi souligné que "l'ancien Levothyrox devrait normalement disparaître puisque le laboratoire ne devrait plus le produire dans les années qui viennent".
"J'aimerais remercier la ministre qui a fait preuve d?une honnêteté rare chez les politiques. Au lieu de nier ou démentir en bloc, elle a admis qu?elle ne savait pas pourquoi il y a avait ces effets et a ordonné une enquête poussée", a réagi auprès du Parisien l'actrice Anny Duperey, qui fait partie des patients ayant porté plainte. "Nous demandons toujours d?avoir le choix entre l?ancienne et la nouvelle formule, et pas seulement pour une période temporaire", a-t-elle toutefois ajouté.
"C'est un premier pas", a réagi auprès de l'AFP Chantal L'Hoir, présidente de l'Association française des malades de la thyroïde (AFMT), qui "reçoit en moyenne 1.000 dossiers de plaignants par jour".
L'ANSM avait réclamé une nouvelle formule du Levothyrox à Merck dès 2012 afin, selon elle, de rendre le produit plus stable. La teneur en lévothyroxine, le principe actif, pouvait en effet varier d'un lot à l'autre, voire au sein du même lot avec le temps. La France est le premier pays où cette nouvelle formule a été introduite mais, selon le laboratoire, des procédures d'homologation sont en cours ailleurs.
Outre l'enquête judiciaire, et une procédure engagée devant la justice administrative à Montpellier, une enquête de pharmacovigilance a été lancée par l'ANSM, qui doit rendre publiques ses conclusions en octobre.
AFP